Pourquoi diantre se préoccuper du méthane, tout d’abord ?
Bien que « on » se focalise souvent sur le seul CO2 quand « on » parle de gaz à effet de serre, il n’en reste pas moins que le CO2 n’est pas le seul de ces gaz à être mis dans l’atmosphère par l’homme : environ un tiers de nos émissions se compose d’autre chose, et dans cet « autre chose » une bonne moitié est due au méthane.
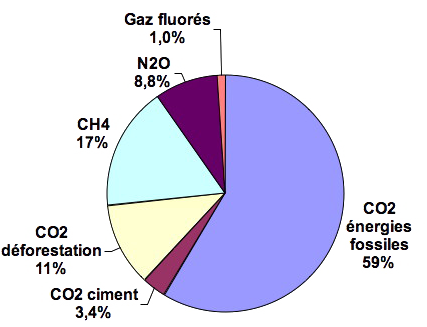
Répartition approximative des émissions humaines de gaz à effet de serre par gaz, en pourcentage, hors ozone, pour l’année 2000.
Source : GIEC
Or le méthane, comme le CO2, est aussi un gaz « naturel » à effet de serre, en ce sens que, avec ou sans hommes, il y a du méthane dans l’atmosphère. Ce que nous avons fait durant les 2 siècles écoulés n’est pas d’avoir mis du méthane dans une atmosphère qui n’en comportait pas, mais d’avoir augmenté la quantité de méthane qui s’y trouvait.
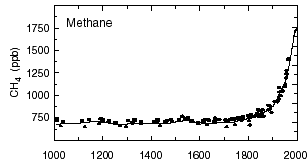
Concentration atmosphérique en méthane depuis l’an mil, en parties par milliard (une partie par milliard = un millilitre pour 1000 m³).
Source : GIEC
Dire qu’il y a naturellement du méthane dans l’atmosphère, c’est donc dire qu’il y a des sources de méthane qui ne viennent pas de l’homme. Et s’il y a de telles sources, il devient alors légitime de se demander si un début de changement climatique ne risque pas d’augmenter les émissions « naturelles » de méthane, exactement comme cela pourrait être le cas avec le CO2. Accessoirement, dire que cette concentration était stable avant l’intervention des hommes, c’est aussi dire qu’il y a des mécanismes naturels d’épuration, sinon les sources naturelles feraient grimper la concentration jusqu’à l’infini, ce qui assurément n’est pas le cas !
La même question de l’influence du climat se pose donc aussi pour les « puits » naturels, où il est tout aussi légitime de se demander si un début de changement climatique affaiblit, renforce, ou ne modifie pas l’épuration de l’atmosphère en méthane. Nous pouvons commencer par la fin, et donner dès à présent la réponse à cette dernière question, car c’est la plus facile : un climat modifié n’aura hélas que peu d’influence sur l’oxydation lente du méthane dans l’atmosphère, qui est la manière dont il en est évacué.
D’où vient le méthane « naturel » et comment peut-il se transformer en hydrates ?
Pour qu’apparaisse du méthane, qui se compose uniquement de carbone et d’hydrogène (et dont la formule, mais ne le répétez à personne, est CH4), il faut qu’un composé organique (un reste animal ou végétal) se décompose à l’abri de l’oxygène de l’air, en suivant une série de transformation permises par la présence de bactéries. En effet, si de l’oxygène passe par là, le carbone et l’hydrogène ont une telle envie de se jeter dessus (la chimie, c’est torride, hein !) qu’il se forme surtout du dioxyde de carbone et de l’eau, et non des hydrocarbures, dont le méthane est un des représentants.
De ce fait, les endroits « naturels » par excellence où il est possible de préserver des détritus organiques de l’oxygène de l’air sont sous l’eau, et sous la terre. Un premier endroit qui correspond très bien au cahier des charges est un marécage, car les restes des plantes qui ont poussé au-dessus du marécage ou à proximité y tombent et se décomposent à l’abri de l’oxygène de l’air. Un feu follet, ce n’est rien d’autre que du méthane formé au fond des marécages qui s’enflamme spontanément au contact de l’oxygène de l’air. Et de fait, la teneur en méthane dans l’air, sur de longues périodes, est un bon marqueur de la pluviométrie globale, car les zones humides ont tendance à être plus étendues lorsque le climat est plus humide. Comme un climat plus humide est aussi un climat plus chaud, il est assez logique de retrouver une concentration atmosphérique en méthane plus élevée lorsque le climat est plus chaud, comme en attestent les carottages effectués dans la glace des pôles.
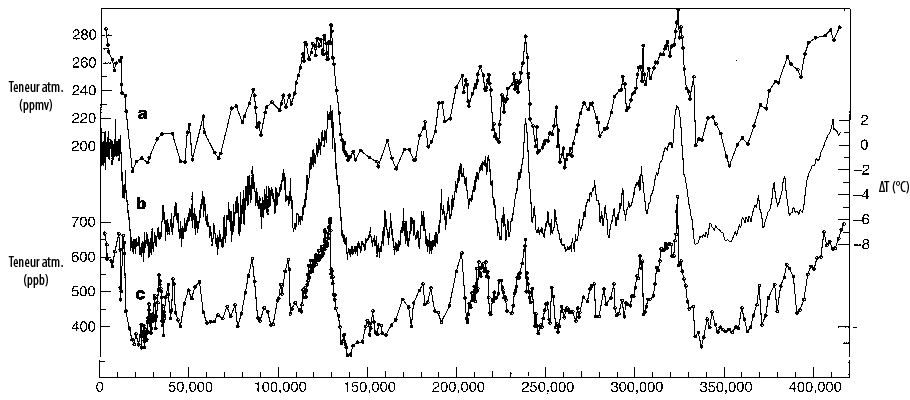
Évolutions comparées sur les 400.000 dernières années (sauf le dernier siècle qui n’est pas représenté) :
- Courbe du haut, de la teneur atmosphérique en CO2, en parties par million – en abrégé ppmv. L’échelle est en haut sur l’axe vertical de gauche
- Courbe du milieu, de la teneur atmosphérique en méthane (CH4) en parties par milliard – en abrégé ppb. L’échelle est en bas sur l’axe vertical de gauche.
- Courbe du bas, de la différence par rapport à maintenant de la température moyenne au niveau du sol en Antarctique (qui est bon marqueur de la température terrestre moyenne). L’échelle est sur l’axe vertical de droite.
Les périodes glaciaires correspondent à des températures et concentrations en CO2 basses, et les âges interglaciaires (comme celui que nous vivons actuellement) correspondent à des valeurs plus élevées de la température et du CO2.
Source : Petit & al., Nature, 1999
Mais il n’y a pas que les marécages qui engendrent la formation de méthane : les sédiments océaniques et le sous-sol sont aussi des sources de méthane, dès lors que s’y trouvent des composés organiques, qui se décomposent plus ou moins lentement à l’abri de l’oxygène de l’air, sous l’effet de bactéries qui sont présentes un peu partout.
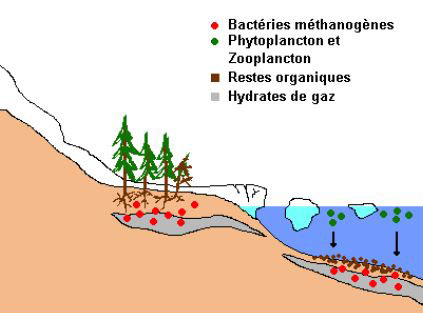
Schéma de la formation des hydrates de méthane.
Une fois formé « naturellement », le méthane peut, ou non, partir rapidement dans l’atmosphère, selon son endroit d’apparition. S’il se forme dans des marécages, il va bien sûr immédiatement partir dans l’air (ce qui explique que la quantité « naturelle » de méthane dans l’air soit un bon marqueur de l’étendue des zones humides), mais pour les autres sources le méthane peut se former sans migrer ensuite dans l’atmosphère à bref délai : les réservoirs de gaz naturel ne sont rien d’autre que du « vieux » méthane qui ne s’est jamais échappé de terre après sa formation dans le sous-sol.
Dans tous les cas de figure, bien sûr, ce méthane va chercher à migrer vers la surface, sous l’effet de la pression qui s’exerce sur lui, et qui est d’autant plus forte qu’il s’est formé profond dans les entrailles de la terre. Mais sa course éperdue vers la surface peut être arrêtée dans un certain nombre de cas de figure :
- s’il est « piégé » par une couche imperméable (en général il s’agit alors de la composante gazeuse d’un réservoir d’hydrocarbures, voir formation du pétrole et du gaz),
- s’il rencontre de l’eau, des fortes pressions, et qu’il ne fait pas trop chaud : il peut alors s’associer à de l’eau (pour cela il faut que l’eau « sature », c’est à dire que le méthane ne puisse plus se dissoudre dans l’eau, ce qui est ce qui se passe si la quantité de méthane est très petite) et former un cristal mixte d’eau et de méthane, qui s’appelle… un hydrate de méthane (on retrouve la même racine « hydrat » que ce que l’on peut lire sur les brumisateurs d’eau ou les crèmes… hydratantes pour les mains). A l’œil, cela ressemble à de la glace (sauf que c’est de la glace qui brûle !).
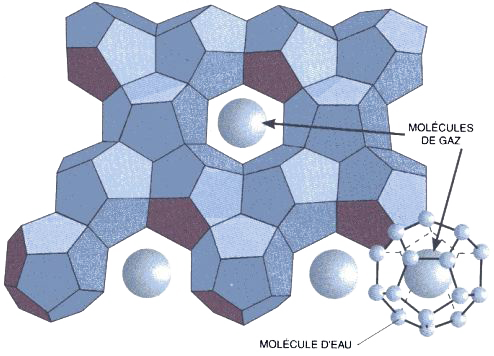
Représentation schématique d’un des types possibles d’hydrate de gaz.
Les molécules d’eau forment un cristal de glace (une structure solide, donc) composé de dodécaèdres réguliers, et l’intérieur de chaque dodécaèdre est occupé par une molécule de gaz retenue prisonnière. Si le gaz retenu prisonnier est du méthane, ce dernier représente à peu près 20% de l’ensemble en poids.
La forme de la « boîte » – faite de molécules d’eau – qui retient le gaz prisonnier peut être un peu différente si le gaz a une molécule plus volumineuse (éthane, butane, etc).
Ce processus de transformation du méthane en hydrate peut notamment se produire :
- sous le sol gelé en permanence des hautes latitudes, qui s’appelle le pergélisol,
- dans les sédiments océaniques.
Sous le pergélisol, la zone où des hydrates sont susceptibles de se trouver est constituée d’une couche de quelques centaines de mètres d’épaisseur qui « démarre » à 200 ou 300 m sous la surface.
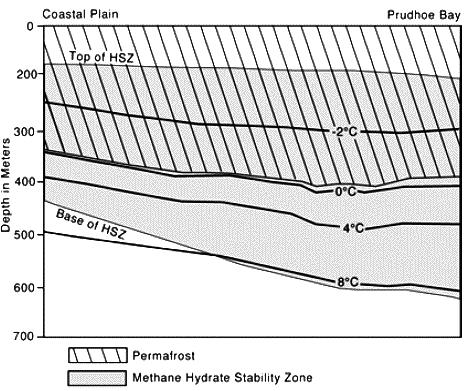
Exemple de zone qui recèle potentiellement des hydrates de méthane dans le pergélisol. HSZ signifie « Hydrate Stability Zone » ; il s’agit de la zone où les conditions de température et de pression permettent de trouver des hydrates (voir détails plus bas).
Le fait que la température remonte quand on s’enfonce dans le sous-sol est normal, et vient de la chaleur géothermique.
Source : M. D. Max, Hydrate ressource for planetary habitation, 2001
Mais l’essentiel du méthane retenu « sous terre » sous forme d’hydrates semble se trouver dans les sédiments océaniques (si l’on fait exception des gisements de gaz naturel, bien sûr !). Ce méthane résulte, comme toujours, de la décomposition des débris animaux et végétaux (essentiellement du phytoplancton et du zooplancton) qui précipitent au fond des océans, où ils sont recouverts par les précipitations minérales (par exemple les débris des coquilles du plancton) puis entraînés vers les entrailles de la terre (voir détails sur la page « formation du pétrole »).
Combien d’hydrates sous nos pieds (et sous les nageoires des dauphins)?
Maintenant que nous savons ce qu’est un hydrate de méthane et comment il se forme, vient la question de la quantité globale de ce composé sur terre, car c’est à partir de là que nous pourrons estimer les risques liés à un largage rapide de tout ou partie de ce méthane dans l’atmosphère. Or répondre à cette question à 100 euros (en fait à beaucoup plus comme nous allons le voir !) est tout sauf une affaire triviale. Une première chose que l’on peut faire pour progresser vers la lumière est « d’éliminer » les endroits où il ne peut pas y avoir d’hydrates, ou pas beaucoup, parce qu’un des ingrédients de la recette n’est pas disponible :
- il ne peut pas y en avoir si la pression est trop faible, ce qui exclut les trop faibles profondeurs d’eau, et en particulier l’essentiel des plateaux continentaux, sauf dans les régions polaires
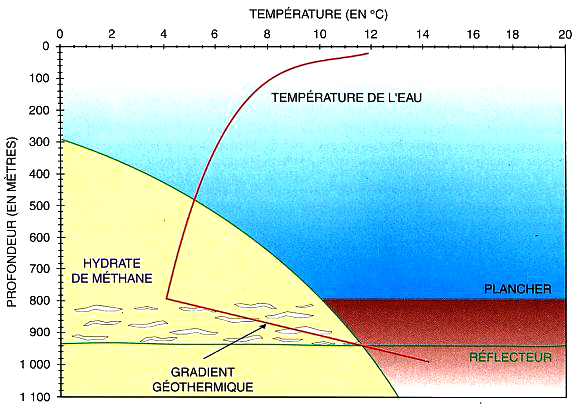
Quelles sont les zones où il va être a priori possible (ou impossible) de trouver des hydrates?
- la courbe rouge intitulée « gradient géothermique » représente la température moyenne de l’eau sous la surface de l’océan, à des latitudes moyennes (en fait, quelle que soit la latitude, la température de l’eau à quelques centaines de mètres de profondeur est presque la même, à quelques degrés près), puis des premières centaines de mètres de sédiment.
L’axe horizontal du haut donne la température, l’axe vertical de gauche la profondeur approximative.
La température commence par baisser à mesure que l’on plonge, en fait tant que l’on reste dans l’eau (car de moins en moins d’énergie solaire chauffe l’eau), puis se met à augmenter quand on descend dans le sol à cause de la chaleur géothermique, qui se dissipe mal en milieu solide, et permet donc une accumulation thermique quand on se rapproche de la source.
- La zone colorée en jaune est la zone de stabilité potentielle des hydrates, délimitée par une courbe donnant la température maximale qui permet l’apparition d’hydrates selon la profondeur (qui donne la pression : chaque 10 m d’eau en plus rajoute l’équivalent de la pression atmosphérique).
Pour des raisons physiques (c’est de la thermodynamique), il est impossible que des hydrates puissent exister à droite de cette courbe. On peut lire cette dernière de deux manières, en se référant à la température (axe horizontal, en haut) ou à la profondeur (c’est-à-dire à la pression, axe vertical à gauche).
Par exemple, pour une température de 4 °C, on peut trouver des hydrates à partir de 450 m de profondeur, mais au-dessus de cette valeur la pression n’est pas assez forte pour que ce cristal mixte puisse se former (il n’y a donc pas d’hydrates dans les régions du globe où la température de l’eau est supérieure à 4°C et la profondeur inférieure à 450 m). Lue dans « l’autre sens », la courbe qui délimite cette zone indique que, à 800 m de profondeur, on peut éventuellement trouver des hydrates tant que la température est inférieure à 10 °C, mais plus ensuite, etc.
Comme les hydrates ne peuvent rester que dans les sédiments (ce composé est moins dense que l’eau, donc s’il apparaît dans l’eau ou qu’il y migre depuis les sédiments il remonte vers la surface en se désagrégeant), on peut donc en trouver entre le plancher océanique, et la profondeur à laquelle la température est suffisamment remontée pour que l’on « sorte » de la zone de stabilité. C’est ce qui arrive à la profondeur dans les sédiments matérialisée par l’intersection entre la courbe « gradient » et la limite de la zone jaune. La limite inférieure des hydrates, dans les analyses sismiques, engendre un écho particulier qui ressemble à celui du fond de l’océan, ce qui explique le terme « réflecteur » mentionné sur ce dessin.
Source : USGS, 2005
- Il ne peut pas y en avoir beaucoup quand il y a de très grandes profondeur d’eau, tout simplement parce que, à quelques exceptions près, il y a peu de vie marine dans l’océan du large, donc peu de plancton qui sédimente au-dessus des grandes profondeurs d’eau, et donc peu de méthane dans le sédiment. Or le méthane doit avoir saturé l’eau dans lequel il est dissous pour que se forme de l’hydrate.
Il résulte de ce qui précède que, pour l’essentiel, les hydrates sont supposés être sur les talus continentaux, ces zones qui plongent des plateaux continentaux vers les abysses, et où la profondeur d’eau est de quelques centaines de mètres, sauf pour les zones polaires où il peut aussi y en avoir sur les plateaux continentaux (mais il faut quand même 300 mètres d’eau au moins comme le rappelle la figure du haut de l’encadré ci-dessus).
Quand il y a une suspicion de trouver des hydrates de méthane quelque part, comment faire pour en avoir le cœur net ? La première technique, peu précise mais utilisée pour « ratisser large », est la sismique. En effet, les hydrates ont une conductivité du signal sonore très largement supérieure à celle du sédiment « ordinaire », de telle sorte que quand un fond contient des hydrates en quantité notable l’écho de la zone contenant ces hydrates est plus faible que celui du reste des sédiments. En plus, le bas de cette zone (qui est le bas de la zone de stabilité des hydrates, à cause de la chaleur des entrailles de la terre, comme expliqué ci-dessus) engendre un écho très caractéristique qui ressemble fortement à celui du fond de l’océan.
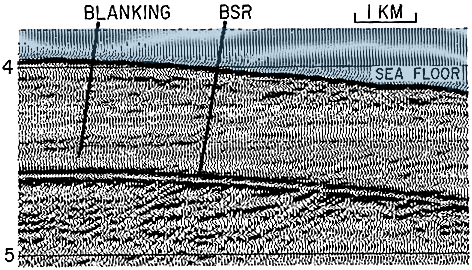
Exemple d’écho obtenu lors d’analyse sismique des fonds marins où la présence d’hydrates de méthane est suspectée. Les chiffres à gauche représentent le nombre de secondes qui séparent l’émission du signal de la réception de l’écho.
Deux « frontières » engendrent un écho quasiment identique : le plancher océanique (Sea Floor), et le bas de la zone de stabilité des hydrates (BSR, pour Bottom Simulating Seismic Reflexion, ou autrement dit « simulation de fond marin »).
Source : USGS, 2005
Ensuite, quand la sismique a permis de repérer une zone qui pourrait bien contenir des hydrates, il faut faire des trous, comme souvent en géologie. Le trou en question, effectué au fond de l’océan, sert à 2 choses :
- il sert d’abord à prélever une carotte, bien sûr, dans laquelle on va chercher à voir s’il y a ou s’il y a eu des hydrates. Mais les « hydratologues » partent avec un sérieux handicap par rapport à tous leurs collègues qui font des trous au fond de l’océan. En effet, pour ces derniers, ce qui est remonté à bord du bateau est identique à ce qui a été prélevé dans les fonds. Pour les hydrates, pas de chance ! comme la pression baisse en cours de remontée du sédiment, l’hydrate sort de sa zone de stabilité et se dissocie partiellement. De la sorte, ce que l’on voit dans la carotte remontée n’est pas identique à ce qui a été prélevé, et il n’est même pas facile de savoir « combien différente » la carotte était au fond de l’eau par rapport à ce que l’on voit sur le pont du bateau !
- le trou sert ensuite – ou en même temps qu’il est fait – à y promener des instruments divers, pour mesurer la résistivité du sédiment en place, l’émission d’infrarouges du même sédiment, et encore quelques autres petites babioles, qui fourniront autant d’indications précieuses pour savoir si des hydrates sont présents tout le long de la carotte, quand bien même ils auraient partiellement disparu quand le prélèvement sera remonté à bord du bateau.
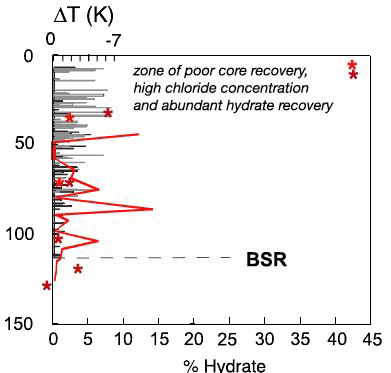
Exemple d’analyses effectuées par des instruments « promenés » dans le trou effectué par un carottier au fond de l’océan, ou effectuées le long de la carotte remontée.
L’axe vertical de gauche indique la profondeur, en mètres, sous le fond de l’océan.
BSR signifie encore Bottom Simulating Seismic Reflexion.
- Les étoiles rouges indiquent la quantité d’hydrates trouvés dans le sédiment remonté par le carottier (qui est un modèle spécial qui « remonte tout » dans un tube étanche) ; l’échelle est donnée par l’axe horizontal du bas,
- les barres grises représentent les anomalies de température mesurées dans le trou par une caméra à infrarouges, car un refroidissement local correspond à une dissociation d’hydrate (échelle du haut, K = kelvin),
- la ligne rouge représente la concentration en chlore dans l’eau contenue dans les pores du sédiment, et c’est un marqueur de la présence d’hydrates, car la formation de ces derniers s’accompagne le plus souvent de l’expulsion de sels chlorés qui se dissolvent ensuite dans l’eau.
Source : Anne Tréhu et al., Joides Journal, 2003
Comme on le voit, même en faisant des trous, savoir exactement combien il y a d’hydrates dans ce qui est prélevé n’est pas nécessairement trivial. En plus, les carottages seuls présentent une limitation importante dans un milieu solide : on peut très bien passer d’une concentration très forte à une concentration quasi-nulle en quelques kilomètres. C’est le cas pour à peu près tout minerai de métal, pour une veine de charbon, ou encore… pour la teneur en carbone du sol (qui peut varier d’un facteur 10 en parcourant moins d’un kilomètre à l’intérieur de la forêt de Fontainebleau !).
La technique appliquée pour les composés dissous dans un fluide (je fais quelques prélèvements, puis j’extrapole à l’ensemble du fluide) ne sont donc plus valables pour donner un ordre de grandeur pour des milieux solides. Cela étant, les carottages, même avec leurs défauts, sont quand même indispensables, car ils représentent le seul moyen d’aller voir ce qui se passe de près, outre qu’ils permettront d’étalonner les outils d’analyse sismique, lesquels peuvent par contre permettre d’estimer des concentrations moyennes sur de larges zones.
Il résulte de ce qui précède (phrase favorite des « matheux » !) que pour obtenir une bonne idée de la quantité d’hydrates stockée dans les fonds marins il faudrait idéalement forer tous les 10 mètres pour l’ensemble de l’océan, avec un carottier qui ne laisse rien échapper de ce qui est remonté. Comme les carottiers qui permettent de conserver l’intégralité du méthane présent dans le sédiment ne datent que de 2002, le lecteur comprendra facilement que nous n’y sommes pas encore.
Les évaluations publiées sur la quantité globale d’hydrates de méthane sur terre sont donc obtenues avec des informations parcellaires et doivent être considérées avec prudence. Comme la proportion d’hydrates dans les sédiments qui en contiennent peut varier du tout au tout, de quelques %, disséminés sous forme de petits filets ou nodules de quelques millimètres (cas de figure le plus courant), à plusieurs dizaines de %, en quelques points d’accumulation particuliers, il est facile de comprendre que l’hypothèse retenue pour le taux moyen d’hydrates dans les sédiments peut faire varier les estimations globales d’un facteur 10 !
Une première synthèse possible de l’information disponible est tout simplement de cartographier les endroits où des hydrates ont été prélevés, ou sont probablement présents au vu des analyses effectuées (ci-dessous).
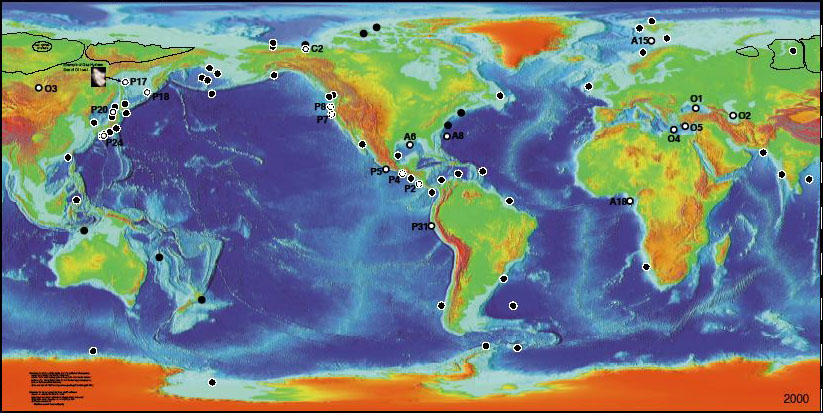
Régions du monde où la présence d’hydrates est avérée par des prélèvements (ronds vides) ou supposée par le biais d’analyses sismiques ou d’analyses de puits dans lesquelles des carottes ont été prélevées (ronds pleins).
Source Keith A. Kvenvolden and Thomas D. Lorenson, USGS, 2000
A partir des informations disponibles, des chercheurs de l’USGS (US Geologic Survey) ont évalué le stock d’hydrates sur terre à 10.000 milliards de tonnes de carbone (le carbone représente les 12/16è du poids total du méthane), soit l’équivalent du double de l’ensemble du gaz, du pétrole et du charbon extractibles de la planète. Encore une fois, il s’agit d’un résultat à considérer avec prudence, et s’il y a peut-être là matière à quelques inquiétudes pour le climat, comme nous allons le voir, rien n’indique qu’une quantité quelconque de ces hydrates soit commercialement exploitable à l’avenir.
Pourquoi est-ce un problème pour le climat, tout ça ?
Comme le méthane est un gaz à effet de serre, et que par ailleurs c’est le principal composant du gaz naturel (et donc qu’il brûle !), il y a deux évolutions liées à ces hydrates qui pourraient avoir une influence – négative – sur le climat :
- si ces hydrates sont commercialement exploitables, l’homme sera tenté d’y puiser une nouvelle source d’énergie carbonée pour faire face à la diminution des autres ressources, par exemple le pétrole, et le recours à ces hydrates comme source d’énergie permettra d’avoir des émissions croissantes de CO2 pendant plus longtemps (en fait certains scénarios d’émission très intensifs en gaz supposent nécessairement que ces hydrates seront exploités),
- que ces hydrates soient commercialement exploitables ou pas, si la zone où ils se trouvent se réchauffe, ils vont cesser d’être stables, se dissocier, et le méthane s’échappera vers l’atmosphère, contribuant alors à accélérer le réchauffement climatique, puisque le méthane est un gaz à effet de serre.
Le premier cas de figure suppose – bis repetita ! – que les hydrates seront commercialement exploitables à large échelle « un jour ». Si leur concentration dans le sédiment ne dépasse pas quelques % en règle générale, rien n’est moins sûr, car il n’est en rien certain que l’on parviendra à trouver un moyen de « ratisser » un milieu solide (les sédiments océaniques) pour en extraire un composé présent à quelques % tout en dépensant moins d’énergie pour ce faire que celle contenue dans le méthane récolté.
Admettons cependant que les endroits où ces hydrates sont suffisamment concentrés soient en nombre tel qu’une bonne fraction de ce composé pourrait servir de source d’énergie. Pouvons nous donner une limite haute aux émissions qui en découleraient ? Si la quantité globale d’hydrates des fonds océaniques est de l’ordre de quelques milliards de tonnes de carbone (c’est une première hypothèse), et si quelques dizaines de % sont extractibles (c’est une deuxième hypothèse), nous nous trouvons là en présence d’une ressource du même ordre de grandeur que le charbon. Or rien qu’avec le charbon nous avons déjà de quoi tellement changer le climat qu’il serait sage d’en laisser la plus grande part sous terre (du charbon), aux possibilités de séquestration près. Ajouter les hydrates au charbon, parce que ce dernier viendrait à manquer, c’est probablement l’assurance de largement dépasser 10°C de hausse de la température planétaire. Serait-ce seulement possible sans que la perturbation du climat ne se charge de nous « calmer » bien avant ?
Même si nous les laissons sous terre (ou sous l’océan), cependant, nous ne pouvons nous désintéresser de ces fichus hydrates. En effet, le réchauffement de la surface planétaire que nous avons mis en route, et qui va s’amplifier de toute façon à l’avenir (mais plus ou moins en fonction de nos émissions, quand même !) va également se propager vers le fond de l’océan, certes très doucement, mais très réellement. Lorsque l’élévation de température se sera propagée jusqu’à la zone de stabilité des hydrates (il faut quand même de l’ordre du siècle), une partie de ceux-ci pourrait se désagréger, et libérer leur méthane qui partira dans l’atmosphère.
La fonte du pergélisol, enfin, pourrait conduire les continents à devenir aussi des sources de méthane : en se propageant lentement vers le bas, l’onde de chaleur engendrera la désagrégation d’une partie des hydrates éventuellement retenus dans le sous-sol des régions arctiques. Le haut de la fourchette, pour l’élévation de température qui pourrait résulter de la libération de méthane des hydrates, dépasse probablement 5 °C, et cela s’ajouterait, bien sûr, à la hausse résultant des émissions directes de l’humanité, et cela s’ajouterait aussi, bien sûr, à la hausse qui pourrait résulter du déstockage rapide du carbone du sol des continents.
Bien sûr, tout cela n’est pas pour demain. Mais comment être sûr que ce n’est pas pour après-demain si nous continuons sur notre lancée ?
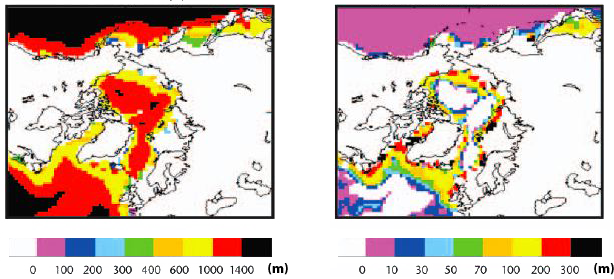
Épaisseur (simulée) de la couche recelant potentiellement des hydrates dans les sédiments autour du Pôle Nord
- à gauche: avec le climat de 1870
- à droite: avec le climat simulé pour l’an 2100 (scénario d’émissions non précisé dans ce résultat).
L’image est centrée sur le pôle : on reconnait le Canada à Gauche et la Sibérie à droite. Par ailleurs les épaisseurs sont représentées avec les mêmes couleurs pour les deux images, bien que l’échelle ne soit pas la même !
Source : Stabilising climate to avoid dangerous climate change – a summary of relevant research at the Hadley Centre, Hadley Centre, 2005